La Organización Mundial de la Salud (OMS) autorizó la primera prueba diagnóstica in vitro de la viruela símica (mpox), siempre y cuando la misma sea utilizada en situaciones de emergencia. En este aspecto, el organismo dio un paso clave para la ampliación del acceso a pruebas de detección de esta enfermedad a nivel mundial.
La prueba Alinity m MPXV, de Abbott Molecular Inc., contribuirá sustancialmente a aumentar la capacidad diagnóstica en países con brotes de esta enfermedad, debido a que la demanda de pruebas rápidas y fiables aumentó drásticamente. El diagnóstico precoz de mpox permite tratar y curar a los pacientes lo antes posible, pudiendo atacar al virus causante.
La importancia de la detección
En África, la capacidad de detección del virus continúa siendo limitada y los casos suelen confirmarse con retraso, favoreciéndose así su propagación. Este año se notificaron más de 30.000 presuntos casos en esta región. En la República Democrática del Congo, uno de los países más afectados, sólo el 37% de casos sospechosos fueron sometidos a pruebas.
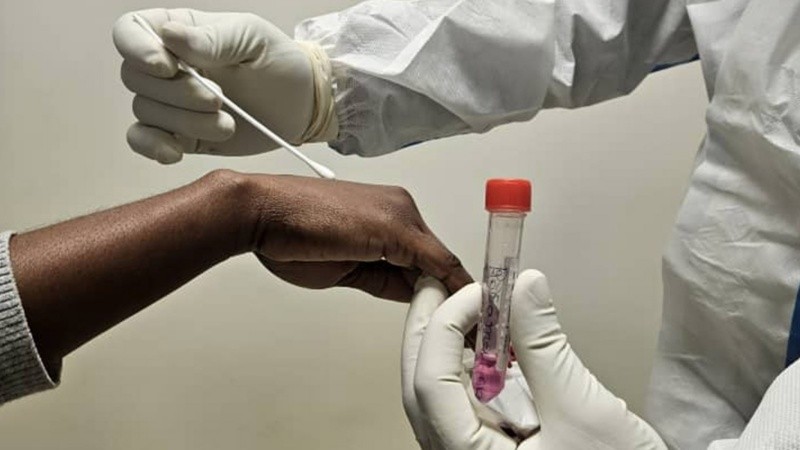
La presencia del virus de mpox se confirma mediante pruebas de amplificación de ácidos nucleicos, como la reacción en cadena de la polimerasa (PCR), ya sea convencional o en tiempo real, como se indica en las orientaciones provisionales de la OMS. Para efectuar esta confirmación diagnóstica en los casos sospechosos se recomienda analizar muestras de las lesiones.
Esta nueva prueba, Alinity m MPXV, una PCR en tiempo real que detecta el ADN de los clados I y II del virus de la mpox en muestras de lesiones cutáneas, debe ser realizada por personal de laboratorio cualificado que conozca las técnicas de PCR y los instrumentos de diagnóstico in vitro. El personal de salud y los técnicos de laboratorio pueden confirmar los casos sospechosos de mpox de manera precisa y eficiente mediante la detección de ADN en muestras tomadas de erupciones de pápulas o vesículas.
Una nueva prueba para utilizar en situaciones de emergencia
La Dra. Yukiko Nakatani, Subdirectora General de la OMS de Acceso a Medicamentos y Productos de Salud, indicó: "La autorización de esta primera prueba diagnóstica de la mpox en el marco del protocolo de uso en emergencias es un paso importante que ayudará a aumentar el cribado en los países afectados. La ampliación del acceso a productos médicos de calidad garantizada es una parte esencial del apoyo que prestamos a los países para contener la propagación del virus y proteger a su población, sobre todo en las zonas desfavorecidas".
El protocolo permite que productos médicos de vital importancia, como vacunas, pruebas diagnósticas y tratamientos, estén disponibles con mayor rapidez ante una emergencia de salud pública de importancia internacional. El 28 de agosto de 2024, la OMS pidió a los fabricantes de pruebas de diagnóstico in vitro de la mpox que solicitaran la autorización de sus productos en virtud del protocolo, ya que la propagación continua del virus obliga a reforzar urgentemente la capacidad mundial de diagnóstico.
Hasta la fecha, la OMS ha recibido otras tres solicitudes de evaluación con arreglo al protocolo de uso en emergencias y continúa en conversaciones con otros fabricantes de pruebas de diagnóstico in vitro de la mpox para ampliar la oferta de medios diagnósticos de calidad garantizada. De esa forma se facilitará que aquellos países que no han autorizado los productos médicos a través de sus procesos internos adquirieran productos que necesitan urgentemente, como estas pruebas diagnósticas, a través de organismos de las Naciones Unidas y otros asociados.
El protocolo que permite el uso de la prueba Alinity m MPXV estará vigente mientras se mantenga la emergencia de salud pública de importancia internacional que justifique el uso en emergencias de pruebas diagnósticas in vitro para detectar la mpox.
Fuente: OMS/WHO.